据统计,全球有超过8160万人长期居住在高海拔地区,同时随着体育、旅游、科研、军事等活动的开展,短期或中期高海拔暴露人群数量也在不断增加。低海拔人类或者动物迁移到高海拔地区后,氧气浓度急速降低会引起机体代偿反应,严重时会导致高原疾病甚至危害生命。研究表明,表型可塑性(例如基因表达可塑性)和遗传进化是低氧适应的两大主要机制。然而由于基因表达的遗传调控在细胞分化过程中以及不同细胞类型之间是动态变化的,我们对基因表达可塑性如何与各种细胞的缺氧耐受性相关仍然知之甚少。在全球气候变化以及由此导致的低氧区域不断涌现的背景下,理解生物体对低氧的响应及其分子和细胞机制尤为重要。绵羊作为一种经典的模式动物和高原地区重要的家畜,为我们探索高原低氧适应性细胞水平的调控机制提供了资源。
近日,中国农业大学动物科学技术学院李孟华教授团队在SCIENCE CHINA Life Sciences上发表题为“Cell-specific gene expression plasticity in response to hypoxia promotes high-altitude adaptive evolution”的原创性研究成果。该研究以绵羊作为动物模型进行“低海拔-高海拔”转移试验,利用10x 单细胞和单细胞核测序技术构建了湖羊在高原转移前和转移后适应过程中的4个时间点(7天、14天、21天和8个月)以及长期适应高原的藏羊的三种关键组织肺、心、脑的单细胞/单细胞核转录组图谱;同时整合单细胞数据和20种测量表型数据在单细胞水平上剖析高原缺氧条件下可塑性与遗传适应之间的关系以及短期高原适应的细胞调控机制。
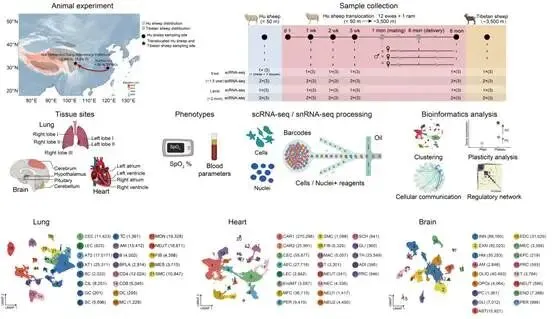
图1 绵羊“低海拔-高海拔”转移试验及分析框架
研究人员基于27只绵羊的肺、心脏和脑组织的27个高分辨率单细胞数据和54个高分辨率单细胞核数据获得了67,869、93,138和75,798个高质量细胞以及255,310、391,717和259,288个高质量细胞核的数据。在此基础上,首次构建了常氧和缺氧环境下绵羊模型重要器官的单细胞转录组图谱,发现一些重要细胞的细胞比例随高原适应而发生明显变化,例如肺中的免疫细胞(如T细胞和B细胞)、心脏中的内皮细胞(如毛细血管内皮细胞)以及脑中的神经元(如兴奋性神经元)在适应过程中不同时间点之间表现出显著的比例变化(P < 0.05)。
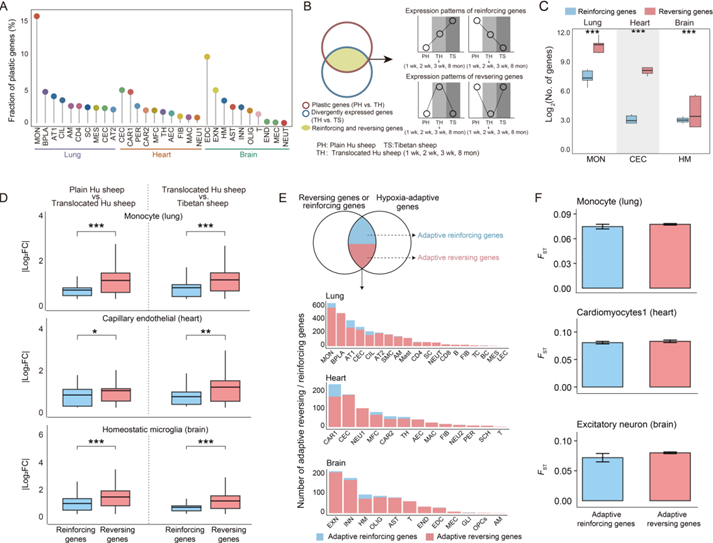
图2 高原低氧适应的细胞基因表达可塑性分析
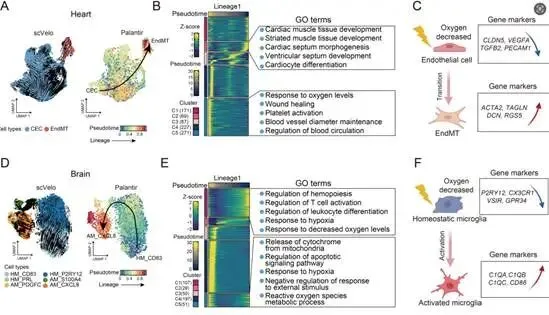
图3 细胞类型转化的拟时序分析
基于以上结果,研究人员揭示了一个潜在的作用于短期和长期低氧适应的细胞调控机制,该机制核心部分是肺、心、脑免疫细胞的缺氧诱导因子HIF以及转录因子AP-1(包含JUN,FOS和ATF等家族,正向调控HIF)和BHLHE41(促进HIF降解)组成的动态调控网络。该机制的另一个主要组成部分是大脑中的稳态小胶质细胞的激活以及血管内皮细胞-EndMT细胞的转化。
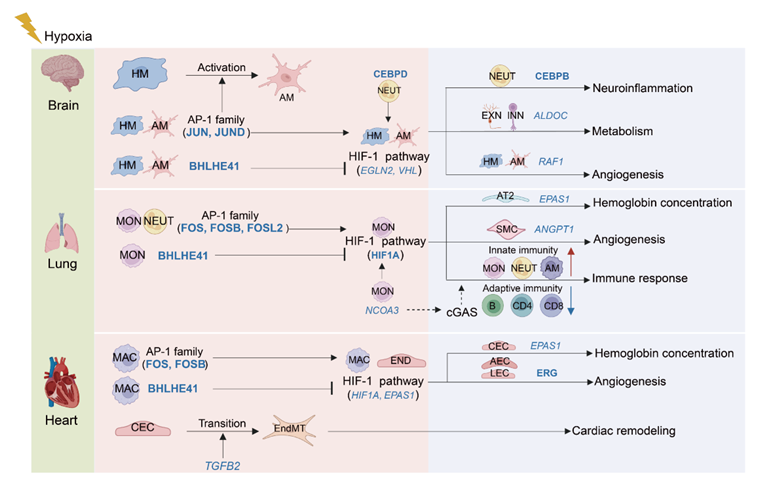
图4 肺、心、脑低氧适应的细胞调控机制
本研究通过整合分析绵羊模型肺、心、脑三个重要器官在常氧和缺氧环境下的单细胞转录图谱,在细胞水平揭示了可塑性与遗传进化的关系以及低氧适应的细胞调控机制。研究结果不仅为理解人类和哺乳动物(如家畜)缺氧适应的关键细胞类型和调控网络提供了新的见解,也为理解缺氧相关疾病的分子和细胞机制提供了重要的参考资源。
中国农业大学为论文第一完成单位,动物科学技术学院李孟华教授和副研究员杨继为论文共同通讯作者,动物科学技术学院博士研究生魏文天、已毕业博士颜泽为论文共同第一作者。本研究获得了国家重点研发计划(2021YFF1000703、2022YFE0113300、2021YFD1300904 和 2021YFD1200900)、国家自然科学基金(32272845 和 32320103006)、中国农业科学院北方农牧业技术创新中心项目(BFGJ2022002)以及国家生物育种重大专项(2023ZD0407106)等项目的资助。
文章链接:https://www.sciengine.com/SCLS/doi/10.1007/s11427-025-3108-3
 微信公众号
微信公众号

